Crizotinib ist ein Arzneistoff zur Behandlung einer bestimmten Form des Bronchialkarzinoms. Er wurde erstmals 2010 vom Pharmaunternehmen Pfizer vorgestellt und ist seit Oktober 2012 unter dem Handelsnamen Xalkori in Europa zur Behandlung der fortgeschrittenen Stadien einer speziellen Unterform des Bronchialkarzinoms zugelassen.
Crizotinib ist ein orales Aminopyridin und als solches ein Tyrosinkinase-Inhibitor, der die ALK-Tyrosinkinase sowie die Tyrosinkinasen MET und ROS1 (c-ros oncogene 1) blockiert. Die Expression der Tyrosinkinase ALK (Anaplastic Lymphoma Kinase) wurde zunächst beim anaplastisch-großzelligen Lymphom und nachfolgend auch bei nicht-kleinzelligen Bronchialkarzinomen sowie bei kindlichen Neuroblastomen beschrieben. Bei Lungenkrebs zeigt sich bei etwa 5 % aller nicht-kleinzelligen Bronchialkarzinome (non small cell lung cancer, NSCLC) eine Translokation dieses Gens, was hochgerechnet jährlich weltweit etwa 60.000 Fällen entspricht.
ALK-positives nicht-kleinzelliges Bronchialkarzinom
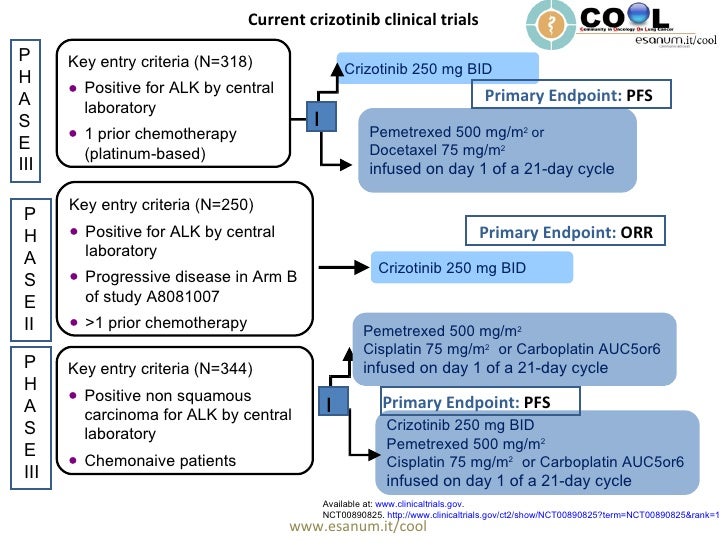
In einer von Pfizer finanzierten multizentrischen offenen Phase-III-Studie zeigte sich 2013 bei 347 eingeschlossenen Patienten mit lokal ausgebreitetem oder metastasiertem ALK-positiven nicht-kleinzelligen Bronchialkarzinom, die vorher bereits eine platinbasierte Chemotherapie erhalten hatten, im Vergleich zu einer weiteren Chemotherapie mit Pemetrexed oder Docetaxel, eine signifikant verlängerte mediane progressionsfreie Überlebenszeit von 7,7 Monaten gegen 3,0 Monaten (Hazardrate 0,49) und eine Wirkung (response rate, als complete response oder partial response) bei 65 % gegen 20 %. Auch die subjektiven Patientenparameter zeigten eine Überlegenheit von Crizotinib gegenüber der Standardtherapie mit stärkerer Symptomreduktion und besserer Lebensqualität. Häufige Nebenwirkungen waren Sehstörungen (60 %), gastrointestinale Störungen mit Durchfall in 60 %, Übelkeit in 55 %, Erbrechen in 47 % und Verstopfung in 42 % sowie erhöhte Leberenzymwerte (38 %). Die meisten Nebenwirkungen waren aber leicht bis mittelschwer (Grad 1–2). Die Nebenwirkungen waren signifikant häufiger und stärker als unter der Standardtherapie, wobei die Behandlung mit Crizotinib aber auch länger durchgeführt wurde. Am 13. Oktober 2015 gab Pfizer bekannt, dass im Zusammenhang mit der Crizotinib-Anwendung ein erhöhtes Risiko für eine Herzinsuffizienz besteht (1,1 % der Behandelten). Todesfälle durch Herzinsuffizienz während einer Therapie mit Crizotinib wurden berichtet.
Am 23. Oktober 2012 wurde Crizotinib durch die Europäische Arzneimittelagentur (EMA), zunächst bedingt, für die Behandlung von Patienten mit ALK-positivem NSCLC zugelassen.
Die Anfang Dezember 2014 publizierte, ebenfalls von Pfizer gesponserte PROFILE 1014-Studie untersuchte die Wirksamkeit von Crizotinib in der first line, d. h. bei bisher chemotherapeutisch unbehandelten Patienten mit ALK-positivem NSCLC. Die Wirksamkeit von 2×250 mg Crizotinib täglich wurde mit einer Standard-Therapie Pemetrexed Cisplatin oder Carboplatin verglichen. Die Beobachtungsdauer der Studie war zu kurz um die mediane Überlebensdauer beurteilen zu können (d. h. der Zeitpunkt, zu dem 50 % der behandelten Patienten im jeweiligen Studienarm verstorben waren, wurde nicht erreicht), jedoch war das progressionsfreie Überleben unter Crizotinib signifikant länger (10,9 Monate, verglichen zu 7,0 Monaten). Die Autoren schlussfolgerten, dass bei ALK-positivem NSCLC Crizotinib der bisherigen Erstlinien-Standardtherapie aus Pemetrexed Carbo- oder Cisplatin überlegen sei.
ROS1-positives nicht-kleinzelliges Bronchialkarzinom (NSCLC)
Bei etwa 2 % der NSCLC liegt ein ROS1-Fusionsprotein vor, das als onkogener Treiber gilt. In den 2010er Jahren wurden mehrere ROS1-Tyrosinkinase-Inhibitor zugelassen: Crizotinib, Entrectinib und Lorlatinib. In der Zulassungsstudie für Crizotinib wurden 50 Patienten mit in 86 % chemotherapeutisch vorbehandeltem ROS1-positivem NSCLC behandelt. Eine komplette Remission erreichten 6 % der Patienten, 66 % eine partielle Remission und bei 18 % war die Erkrankung stabil. Die Gesamt-Ansprechrate lag damit bei 72 %, das mittlere progressionsfreie Überleben lag bei 19,2 Monaten. Die Nebenwirkungen waren vergleichsweise gering.
Jedoch kam es bei 50 % der mit einem Tyrosinkinase-Inhibitoren der ersten Generation behandelten Patienten zu einer Resistenz-Mutation, z. B. als Punktmutation „G2032R“. Ebenso passierten sie kaum die Blut-Hirn-Schranke und hatten so bei den häufigen Hirnmetastasen eine geringe intrakraniale Aktivität, auch wenn sie bei Entrectinib besser war als bei Crizotinib.
Frühe Nutzenbewertung
In Deutschland müssen seit 2011 neu zugelassene Medikamente mit neuen Wirkstoffen gemäß § 35a SGB V einer „frühen Nutzenbewertung“ durch den Gemeinsamen Bundesausschuss (G-BA) unterzogen werden, wenn der pharmazeutische Hersteller einen höheren Verkaufspreis als nur den Festbetrag erzielen möchte. Nur wenn ein Zusatznutzen besteht, kann der Arzneimittelhersteller mit dem Spitzenverband der gesetzlichen Krankenkassen einen Preis aushandeln. Die Dossierbewertungen, auf deren Basis der G-BA seine Beschlüsse fasst, erstellt das Institut für Qualität und Wirtschaftlichkeit im Gesundheitswesen (IQWiG).
In der ersten frühen Nutzenbewertung wurde Crizotinib zur Behandlung Erwachsener mit vorbehandeltem Anaplastische-Lymphom-Kinase (ALK)-positivem, fortgeschrittenem nicht kleinzelligem Bronchialkarzinoms 2013 verglichen mit einer Chemotherapie mit Docetaxel oder Pemetrexed – oder mit Best Supportive Care, falls eine Chemotherapie nicht angezeigt ist. Der G-BA-Beschluss war befristet und wurde 2016 durch einen neuen Beschluss aufgehoben. Demnach gibt es für Patienten, bei denen eine Chemotherapie angezeigt ist, einen Anhaltspunkt für einen beträchtlichen Zusatznutzen. Für Betroffene, bei denen eine Chemotherapie nicht angezeigt ist, ist ein Zusatznutzen nicht belegt.
2016 wurde zudem eine frühe Nutzenbewertung in einem neuen Anwendungsgebiet durchgeführt: der Erstlinienbehandlung Erwachsener mit ALK-positivem, fortgeschrittenem nicht kleinzelligen Lungenkarzinom. Gemäß G-BA-Beschluss gibt es gegenüber Cisplatin in Kombination mit Pemetrexed oder Carboplatin in Kombination mit Pemetrexed einen Anhaltspunkt für einen beträchtlichen Zusatznutzen.
Nachdem Crizotinib auch für die Behandlung Erwachsener mit ROS1-positivem, fortgeschrittenem NSCLC zugelassen wurde, folgte 2016 und 2017 eine weitere Nutzenbewertung. Gemäß G-BA-Beschluss ist in diesem Anwendungsgebiet ein Zusatznutzen weder für nicht vorbehandelte noch für vorbehandelte Patienten belegt.
Einzelnachweise